Vorhofflimmern
- Autor(en): Ramin Ebrahimi, Laurent Haegeli
- pharma-kritik-Jahrgang 41
, Nummer 11, PK1093
Redaktionsschluss: 11. Mai 2020
DOI: https://doi.org/10.37667/pk.2019.1093 - PDF-Download der Printversion dieser pharma-kritik Nummer
Vorhofflimmern ist die häufigste Form von Herzrhythmusstörungen. Sie betrifft derzeit etwa 1-2% der Bevölkerung mit weltweit zunehmender Prävalenz. Allein aufgrund des demographischen Wandels ist eine weitere deutliche Zunahme zu erwarten. Die wichtigsten Elemente der Therapie des Vorhofflimmerns sind eine wirksame Thromboembolie-Prophylaxe sowie eine Rhythmus- oder Frequenzkontrolle.(1) Dieser Artikel soll ein übersichtliches Update der medikamentösen und interventionellen Therapiemöglichkeiten vermitteln.
Indikation zur oralen Antikoagulation
Zur Verhinderung des Auftretens der relevantesten Komplikation des Vorhofflimmerns, eines Schlaganfalls, ist die Indikation einer therapeutischen Antikoagulation zu evaluieren. In den aktuellen Guidelines der European Society of Cardiology (ESC) wird zur Risikoabschätzung der CHA2DS2-VASc-Score empfohlen, siehe Tabelle 1.(2) Daneben werden aktuell weitere Modelle zur Risikoabschätzung eines Schlaganfalls evaluiert (ABC-Score, ATRIA-Score usw.), die Faktoren beinhalten, die im CHA2DS2-VASc-Score nicht berücksichtigt sind. So werden Faktoren wie Biomarker, der «Global Longitudinal Strain» (GLS) des Vorhofs und Faktoren wie Niereninsuffizienz und Proteinurie mit bereits vielversprechenden Ergebnissen untersucht. Jedoch haben diese Ergebnisse noch nicht Aufnahme in die Guidelines gefunden.
Bei einem Score von null Punkten bei Männern und einem Punkt bei Frauen liegen keine guten Daten vor, dass die Vorteile einer oralen Antikoagulation die Risiken überwiegen. Für Männer mit 1 oder Frauen mit 2 Punkten gibt es zunehmende Evidenz für einen Nutzen der oralen Antikoagulation. Ab einem Score von 2 Punkten bei Männern oder 3 Punkten bei Frauen ist von einem signifikant erhöhten Thromboembolie-Risiko auszugehen; in dieser Population wird zu einer therapeutischen oralen Antikoagulation geraten (Klasse I, Evidenzgrad A). Praktisch ist es daher so, dass ein Grossteil der Personen mit einem Vorhofflimmern dauerhaft antikoaguliert werden sollte (und zwar unabhängig davon, ob und mit welchem Erfolg eine Rhythmus- oder Frequenzkontrolle erfolgt). Der Einsatz von Plättchenhemmern zur Thromboembolie-Prophylaxe ist in der aktuellen Leitlinie unabhängig vom Risikoscore nicht mehr vorgesehen, da für deren Wirksamkeit keine Evidenz aufgezeigt werden konnte (Klasse-III-Empfehlung).
Wahl eines Antikoagulans
Mit Apixaban (Eliquis®), Dabigatran (Pradaxa®), Edoxaban (Lixiana®) und Rivaroxaban (Xarelto®) stehen vier direkte, Nicht-Vitamin-K-abhängige orale Antikoagulantien («non-vitamin K antagonist oral anticoagulants», NOACs) zur Schlaganfallprophylaxe zur Verfügung. Diese Medikamente können beim nicht-valvulären Vorhofflimmern (ohne mittelschwere oder schwere Mitralklappenstenose und ohne mechanische Herzklappen) eingesetzt werden. In zahlreichen Studien haben diese Wirkstoffe im Vergleich zu Warfarin (Coumadin®), dem in den randomisierten Zulassungsstudien eingesetzten Vitamin-K-Antagonisten, einen mindestens äquivalenten Schutz vor Schlaganfällen gezeigt. Zudem wurde für die NOACs eine Verminderung von schwerwiegenden Nebenwirkungen (letale Blutungen bzw. intrakranielle Blutungen) im Vergleich zu Warfarin dokumentiert. Dementsprechend wird in den aktuellen europäischen Richtlinien beim nicht-valvulären Vorhofflimmern primär der Einsatz der NOACs empfohlen. Sollte eine mechanische Herzklappe oder eine mittelschwere oder schwere Mitralklappenstenose vorliegen, so wird weiterhin der Einsatz eines Vitamin-K-Antagonisten zur Antikoagulation empfohlen.(1)
Fast alles, was wir zu den Vergleichen von NOACs mit Vitamin-K-Antagonisten wissen, beruht auf Vergleichen mit Warfarin. Warfarin hat jedoch eine andere Kinetik als Phenprocoumon (Marcoumar®) oder Acenocoumarol (Sintrom®). Über mögliche Vorteile der NOACs gegenüber Phenprocoumon und Acenocoumarol wissen wir dementsprechend wenig.
Da vier verschiedene Wirkstoffe innerhalb der Gruppe der NOACs zur Verfügung stehen, besteht die Möglichkeit, eine individualisierte Therapie einzusetzen. Es ist in diesem Rahmen jedoch zu erwähnen, dass keine direkten Vergleichsstudien zwischen den verschiedenen NOACs vorliegen. Bei Vorliegen einer relevanten Niereninsuffizienz ist dennoch vorzugsweise der Einsatz von Apixaban bzw. von Edoxaban oder Rivaroxaban in reduzierter Dosierung ratsam. Liegt eine Anamnese von gastrointestinalen Blutungen vor, so ist Apixaban oder Dabigatran in reduzierter Dosierung vorzuziehen. Weitere Faktoren wie der Wunsch nach der Verfügbarkeit eines zugelassenen Antidots (vorzugsweise Dabigatran) oder der Wunsch nach einer einmal täglichen Einnahme (Edoxaban oder Rivaroxaban) können die Wahl des NOACs ebenfalls beeinflussen.
Interaktionen
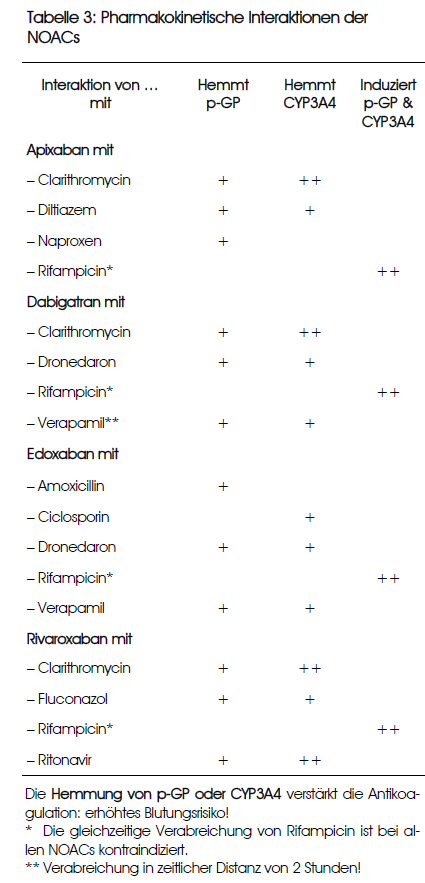
NOACs verursachen weniger gefährliche Interaktionen als die Vitamin-K-Antagonisten. Dennoch können sich problematische Konsequenzen aus pharmakokinetischen Interaktionen der NOACs ergeben, wobei überwiegend Interaktionen mit Transportproteinen – besonders mit P-Glykoprotein (P-gp) – von Bedeutung sind.(3)Namentlich bei Apixaban und Rivaroxaban spielt auch das Zytochrom CYP3A4 eine Rolle. In der Praxis sind vor allem Interaktionen mit Azol-Antimykotika, einzelnen Makroliden und Rifampicin (Rimactan® u.a.) wichtig. Einzelheiten finden sich in der Tabelle 3 (Seite 43).
Sind NOACs kontraindiziert, so ist in der Regel eine orale Antikoagulation mit einem Vitamin-K-Antagonisten möglich. Das Blutungsrisiko wird – wie bei anderen Antikoagulantien – durch die gleichzeitige Verabreichung von Plättchenhemmern, systemischer Steroidtherapie, nicht-steroidalen Entzündungshemmern, Thrombozytopenie oder auch durch die Anamnese einer gastrointestinalen Blutung erhöht.
Korrekte Dosierung
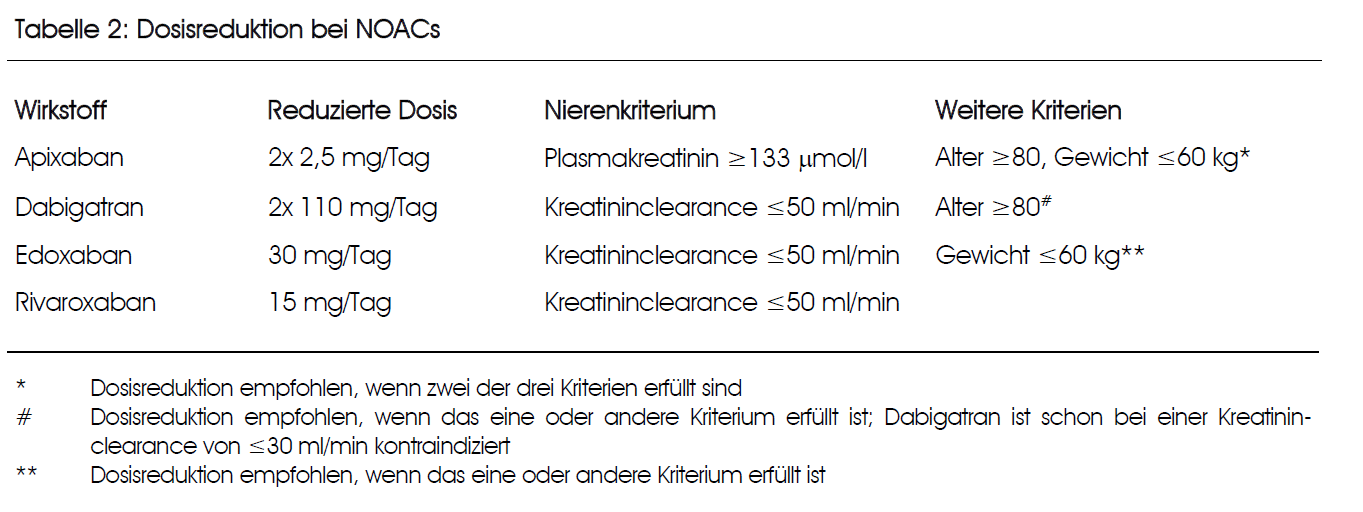
Spezielle Beachtung sollte der Dosierung der verschiedenen Wirkstoffe gewidmet werden (siehe Tabelle 2). Bei schwerer Leberinsuffizienz und bei einer fortgeschrittenen Niereninsuffizienz (Kreatininclearance unter 15 ml/min) sind alle NOACs kontraindiziert. Bei Rivaroxaban ist zudem zu beachten, dass die (beim Vorhofflimmern verwendete) höhere Dosis mit einer Mahlzeit eingenommen werden muss.
Mehrfachhemmung der Blutgerinnung
Jede Kombination von oralen Antikoagulantien und Plättchenhemmern stellt ein erhöhtes Blutungsrisiko dar. Dies gilt auch für die NOACs. Alle entsprechenden Studien haben ein erhöhtes Blutungsrisiko gezeigt (auch für die nur «duale» Kombination – ein Plättchenhemmer zusätzlich zur oralen Antikoagulation).
In den entsprechenden Guidelines der ESC wird bei einem Myokardinfarkt und gleichzeitig vorliegendem Vorhofflimmern die Kombination von zwei Plättchenhemmern – Acetylsalicylsäure (Aspirin Cardio® u.a.) und Clopidogrel (Plavix® u.a.) – mit einem NOAC meist in der niedrigeren zugelassenen Dosis für mindestens einen Monat empfohlen. Je nach Ischämie-Risiko kann diese Dreifach-Therapie sogar bis zu 6 Monate lang fortgeführt werden. Anschliessend sollte vorzugsweise einer der beiden Plättchenhemmer sistiert werden; gleichzeitig ist es jedoch meistens erforderlich, die Dosierung des NOAC auf die normale Dosis anzupassen. Ein Jahr nach dem Myokardinfarkt besteht dann die Möglichkeit, bei fehlenden Hochrisiko-Charakteristika für ischämische Ereignisse mit einer Monotherapie mit einer «normal» dosierten Antikoagulation fortzufahren. Gemäss einer Metaanalyse, in der zwei japanische Studien zusammengefasst sind, verhindern bei einer stabilen koronaren Herzkrankheit NOACs allein kardiovaskuläre Ereignisse ebenso gut wie eine Kombination mit Plättchenhemmern. Die Monotherapie verursacht aber signifikant weniger gefährliche Blutungen.(4) Da die Dreifach-Therapie mit einem deutlich erhöhten Blutungsrisiko assoziiert ist, wird sie in Zukunft möglicherweise schon früh nach dem Infarktereignis auf Fälle mit einem besonders hohen Ischämierisiko beschränkt bleiben.(5) Wichtig ist in diesem Zusammenhang auch, dass die anderen plättchenhemmenden P2Y12-Hemmer Prasugrel (Efient® u.a.) und Ticagrelor (Brilique®) in der Dreifach-Therapie mit Acetylsalicylsäure und NOAC nicht Verwendung finden sollten, da diese Kombination zu einem besonders stark erhöhten Blutungsrisiko führt.
Antidote
Zurzeit ist in der Schweiz nur ein Antidot (Idarucizumab = Praxbind®, gegen Dabigatran) auf dem Markt verfügbar.(6) In anderen Ländern ist mit Andexanet-alpha (Ondexxya®) auch ein Antidot verfügbar, das bei schweren Blutungen unter Apixaban oder Rivaroxaban (eventuell auch unter Edoxaban) verwendet werden kann.
Verschluss des linken Vorhofohrs
Sollte im Anschluss an eine Blutungskomplikation eine eindeutige Kontraindikation für das Fortführen einer medikamentösen therapeutischen Antikoagulation bestehen, so besteht im Sinne einer möglichst effektiven Verhinderung eines thromboembolischen Ereignisses die Möglichkeit des Verschlusses des linken Vorhofohrs.
Hierbei unterscheidet man einen chirurgischen von einem interventionellen Verschluss. Für den chirurgischen Verschluss des linken Vorhofohrs gibt es bisher keine verlässliche Datenlage, die eine adäquate Wirksamkeit im Vergleich zu einer medikamentösen oralen Antikoagulation belegen könnte. Hierzu wird jedoch aktuell eine grosse randomisierte Studie («Left Atrial Appendage Occlusion Study», LAAOS III) durchgeführt. Nach einem chirurgischen Verschluss des Vorhofohrs besteht dementsprechend nach den aktuellen europäischen Guidelines weiterhin eine Klasse-I-Indikation für die Fortführung der oralen Antikoagulation. Besser dokumentiert sind die Resultate der perkutanen Implantation eines «Okkluders». So wurde z.B. für das Watchman-Verschlusssystem in einer randomisierten Studie (PROTECT AF) eine Nicht-Unterlegenheit für thromboembolische Ereignisse im Vergleich zu einer oralen Antikoagulation mit Warfarin gezeigt.(7) In dieser Studie wurden nicht explizit Personen mit einer Kontraindikation für eine orale Antikoagulation eingeschlossen. Dennoch wird im klinischen Alltag von den Studienresultaten auch auf Betroffene mit einer Kontraindikation für eine orale Antikoagulation extrapoliert und ein interventioneller Verschluss des Vorhofohrs angestrebt.(8)
Katheterablation (Pulmonalvenenisolation)
Gemäss den ESC-Guidelines zum Vorhofflimmern besteht bei symptomatischen Personen eine etablierte Indikation für eine Pulmonalvenenisolation. Die Wahl zwischen diesem Eingriff und der medikamentösen Therapie soll jedoch gemeinsam von den verantwortlichen Fachpersonen und den betroffenen Patientinnen und Patienten getroffen werden. Dabei ist eine gute Auswahl der für den Eingriff geeigneten Personen wichtig.
Die Pulmonalvenenisolation ist heute ein Routineeingriff mit einer sehr geringer Rate an relevanten Komplikationen. Dabei werden die Lungenvenen entweder mittels Radiofrequenz-Energie oder mittels Abgabe von Kälte (Kryo-Ablation) oder Laser-Energie zirkumferentiell elektrisch vom linken Vorhof isoliert. In der Regel verbleiben die Behandelten im Anschluss an die Pulmonalvenenisolation für eine Nacht im Spital und werden ambulant nach 3 und 12 Monaten klinisch und mittels 24-Stunden-EKG-Monitoring nachkontrolliert.(9-12)
In der CABANA-Studie («Catheter Ablation vs Antiarrhythmic Drug Therapy for Atrial Fibrillation») hat die Katheterablation im Vergleich zur medikamentösen Therapie den kombinierten Endpunkt (Tod, Schlaganfall, schwere Blutung oder Herzstillstand) nicht signifikant reduziert.(13) Der Eingriff hat jedoch, ebenso wie in der CAPTAF-Studie («Catheter Ablation compared with Pharmacological Therapy for Atrial Fibrillation»), zu klinisch bedeutsamen und signifikanten Verbesserungen der Lebensqualität geführt.(14,15)
Ein weiterer wichtiger Punkt im Management des Vorhofflimmerns ist die Therapie bei Auftreten von Symptomen einer Herzinsuffizienz. Etwa 50% der Erkrankten mit Vorhofflimmern weisen zum Zeitpunkt der Erstdiagnose bereits Symptome einer Herzinsuffizienz auf. Umgekehrt hat ein Drittel der Personen, die aufgrund einer Herzinsuffizienz hospitalisiert werden, ein Vorhofflimmern. Eine oft übersehene Komponente der neu entdeckten Herzinsuffizienz ist die «Tachykardie-induzierte Kardiomyopathie», die auch bei vorbestehenden Erkrankungen wie z.B. koronarer Herzkrankheit die Pumpfunktion oft zusätzlich deutlich verschlechtern kann.
Lange wurde in diesem Setting zwischen den zwei fundamentalen Therapiestrategien der Frequenz- und der Rhythmuskontrolle unterschieden. Bisher konnte aber mit allen rein medikamentösen Therapiestudien nie ein Unterschied zwischen den beiden Strategien in Bezug auf die Mortalität gezeigt werden.
In der CASTLE-AF-Studie führte eine Pulmonalvenenisolation bei etablierter Herzinsuffizienz mit reduzierter Auswurffraktion (LVEF <35%) und implantiertem ICD im Vergleich zu einer medikamentösen Therapie des Vorhofflimmerns zu einer signifikanten Senkung der Mortalität.(16) Diese Ergebnisse müssen aber noch in weiteren Studien bestätigt werden. In der akuten Situation steht die medikamentöse Frequenz- oder Rhythmuskontrolle im Vordergrund.
Bei instabilen Patientinnen und Patienten kann die Rhythmuskontrolle durch die Applikation eines zum QRS-Komplex synchronisierten biphasischen Stromstosses mit 200 J in Kurznarkose erreicht werden. Aktuell sind Personen mit Herzinsuffizienz mit reduzierter Auswurffraktion nicht das Kollektiv der ersten Wahl bei der Entscheidung zur Katheterablation. Bei Kranken mit Herzinsuffizienz und Vorhofflimmern wurde ein interventioneller Ansatz lange eher zurückhaltend gewählt, auch weil die Erfolgsrate der Katheterablation und die Rezidive durch verschiedene Faktoren beeinflusst werden, u.a. durch die Vorhofsgrösse. Weiterhin ist es in diesem Rahmen wichtig, eine gute Selektion vorzunehmen. Weitere Studienergebnisse sind unbedingt erforderlich, da durch die CASTLE-AF-Studie einige Fragen offen geblieben sind.
Antiarrhythmische Medikamente
Obwohl eine medikamentöse Frequenz- oder Rhythmuskontrolle keine signifikanten Unterschiede in Bezug auf die Mortalität gezeigt hat, wird die Rhythmuskontrolle häufig von den Betroffenen als symptomatischer Therapieansatz gewünscht. Alternativ zu einer medikamentösen antiarrhythmischen Therapie kann auch eine Katheterablation durchgeführt werden.
Bei der reinen Frequenzkontrolle wird eine Ruheherzfrequenz von <110/min empfohlen. Bei Personen mit eingeschränkter linksventrikulärer Funktion (LVEF <40%) stehen einerseits Betablocker zur Verfügung, die erst in rekompensiertem Zustand eingesetzt werden sollten und in der Dosierung vorsichtig gesteigert werden sollten. Andererseits besteht in diesen Fällen die Möglichkeit der Gabe von Digoxin (entweder zusätzlich zum Betablocker oder als Alternative zum Betablocker). Bei Betroffenen mit einer LVEF ≥40% und rekompensiertem Zustand stehen Betablocker, Digoxin und die Kalziumantagonisten Verapamil (Isoptin®) oder Diltiazem (Dilzem® u.a.) zur Verfügung. Sollte trotz diesen Massnahmen keine Frequenzkontrolle erreicht werden, so müsste eine «Pace and ablate»-Strategie diskutiert werden. Dabei wird in einem ersten Schritt bei eingeschränkter linksventrikulärer Funktion vorzugsweise ein CRT-P («Cardiac Resynchronization Therapy-Pacemaker») implantiert und in einem zweiten Schritt in der Regel vier Wochen nach der Implantation eine AV-Knoten-Ablation vorgenommen.(1)
Literatur
- 1) Freedman B et al. Lancet 2016; 388: 806-17
- 2) Kirchhof P et al. Eur Heart J 2016; 37: 2893-62
- 3) Herink MC et al. Drugs 2019; 79: 1625-34
- 4) Kheiri B et al. J Thromb Thrombolysis 2020 (Jan 24); doi: 10.1007/s11239-020-02041-7
- 5) Massberg S et al. Dtsch Med Wochenschr 2018; 143: 1090-3
- 6) Röllin A. pharma-kritik 2016; 38: 45-7 (pk1012)
- 7) Fountain RB et al. Am Heart J 2006; 151: 956-61
- 8) Kramer DB et al. N Engl J Med 2015; 372: 994-5
- 9) Haegeli LM et al. Eur Heart J 2014; 35: 2454-9
- 10) Jud FN et al. Anatol J Cardiol 2019; 21: 142-9
- 11) Haegeli L et al. Eur Heart J 2015; 36: 255-64
- 12) Själander S et al. JAMA Cardiol 2017; 2: 146-52
- 13) Packer DL et al. JAMA 2019; 321: 1261-74
- 14) Mark DB et al. JAMA 2019; 321: 1275-85
- 15) Blomström-Lundqvist C et al. JAMA 2019; 321: 1059-68
- 16) Marrouche NF et al. N Engl J Med 2018; 378: 417-27
Standpunkte und Meinungen
- Es gibt zu diesem Artikel keine Leserkommentare.
Copyright © 2024 Infomed-Verlags-AG
PK1093
Verwandte Artikel
Gratisbuch bei einem Neuabo!
pharma-kritik abonnieren
-
Jahrgang 45 / 2023
Jahrgang 44 / 2022
Jahrgang 43 / 2021
Jahrgang 42 / 2020
Jahrgang 41 / 2019
Jahrgang 40 / 2018
Jahrgang 39 / 2017
Jahrgang 38 / 2016
Jahrgang 37 / 2015
Jahrgang 36 / 2014
Jahrgang 35 / 2013
Jahrgang 34 / 2012
Jahrgang 33 / 2011
Jahrgang 32 / 2010
Jahrgang 31 / 2009
Jahrgang 30 / 2008
Jahrgang 29 / 2007
Jahrgang 28 / 2006
Jahrgang 27 / 2005
Jahrgang 26 / 2004
Jahrgang 25 / 2003
Jahrgang 24 / 2002
Jahrgang 23 / 2001
Jahrgang 22 / 2000
Jahrgang 21 / 1999
Jahrgang 20 / 1998
Jahrgang 19 / 1997
Jahrgang 18 / 1996
Jahrgang 17 / 1995
Jahrgang 16 / 1994
Jahrgang 15 / 1993
Jahrgang 14 / 1992
Jahrgang 13 / 1991
Jahrgang 12 / 1990
Jahrgang 11 / 1989
Jahrgang 10 / 1988
Kennen Sie "100 wichtige Medikamente" schon?
Die Liste der 100 Medikamente sehen Sie auf der Startseite von 100 Medikamente.